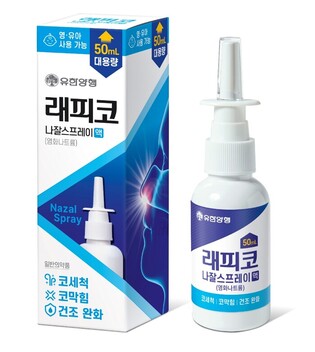
셀트리온은 이달 13일(현지시간)까지 미국 뉴올리언스에서 열린 미국암연구학회(AACR)에서 항암제 '아바스틴(성분명 베바시주맙)'의 바이오시밀러 'CT-P16'의 임상 3상 시험 결과를 최초 공개했다고 13일 밝혔다.
 |
| ▲ [셀트리온 CI] |
셀트리온은 이번 발표를 통해 아바스틴의 대표 적응증인 비소세포폐암 환자 689명을 두 개의 그룹으로 나눠 각각 CT-P16과 아바스틴을 병용 항암제와 3주에 한 번씩 최대 6회에 걸쳐 투약한 뒤 최대 3년간 단독 투약하는 3상 임상 결과를 공개했다.
셀트리온에 따르면, CT-P16은 투약 후 유도 시험 기간에 오리지널의약품 간 객관적반응률의 비교에서 동등성 입증을 위한 한계 구간을 만족해 효능 면에서 동등성을 입증했다.
아바스틴은 다국적 제약사인 로슈가 개발한 블록버스터 항암제로 비소세포폐암을 비롯한 전이성 직결장암, 전이성 유방암, 교모세포종 등의 치료에 쓰인다. 지난해 기준 글로벌 매출은 약 4조 원(30억 5000만 스위스 프랑)에 달한다.
셀트리온은 글로벌 3상 임상 결과를 바탕으로 아바스틴에 승인된 전체 적응증에 대해 한국과 미국, 유럽 등에 CT-P16 품목허가를 신청했다.
아울러 CT-P16이 출시되면 기존 혈액암 치료제 트룩시마와 유방암 치료제 허쥬마에 이어 세 번째 항암 항체 바이오시밀러를 확보하게 된다.
[저작권자ⓒ 메가경제. 무단전재-재배포 금지]